

开云官网登录平台
经济日报-我国经济网7月15日讯(记者朱国旺郭文培)几天前,江苏吴中实业股份有限公司(以下简称江苏吴中)对外公告,公司相继收到我国食品药品检定研究院、河南省食品药品查验所关于注射用硫酸阿米卡星不合格的陈述,正在召回不合格产品。7月14日,江苏吴中再次发布关于注射用硫酸阿米卡星抽检不合格的公告,与以往不必的是,此次公告称,公司注射用硫酸阿米卡星已被江苏省药品监管局责令停产。
早在7月4日,江苏吴中就曾对外公告,所属江苏吴中医药集团有限公司姑苏制药厂(以下简称“苏药厂”)于7月3日收到了《我国食品药品检定研究院查验陈述》,苏药厂出产的8批次(批号:1910094、1910124、1912044、1912054、1912064、1912074、1912094、1912104)注射用硫酸阿米卡星(0.2g)抽检不合格,不合格项目为溶液的弄清度与色彩。江苏吴中称,苏药厂已暂停出产并自动召回该药品,到公告日(4日),苏药厂没有收到监管部门的处分、责令整改、停产等监管办法。
7月10日,江苏吴中再次公告,苏药厂于7月8日收到了《河南省食品药品查验所查验陈述》,苏药厂出产的1批次(批号:1905244)注射用硫酸阿米卡星(0.2g)抽检不合格,不合格项目同为溶液的弄清度与色彩。相同,到公告日(7日),苏药厂没有收到监管部门的处分、责令整改、停产等监管办法。
7月14日,江苏吴中再次发布了重要的公告,苏药厂出产的注射用硫酸阿米卡星不合格。与前两则公告不同的是,因出产不符合药品规范的药品注射用硫酸阿米卡星,苏药厂于7月11日收到了江苏省药品监督管理局出具的《责令改正通知书》。江苏省药品监督管理局要求,在不合格的原因查询、定论清晰以及整改办法执行之前,苏药厂立马中止出产、出售药品注射用硫酸阿米卡星。一起,当即召回效期内的一切批次的注射用硫酸阿米卡星,并于7月31日前完结相关改正。
据悉,注射用硫酸阿米卡星系江苏吴中会集收购中标产品,中标价格为0.98-1.739元/瓶。日前,江苏吴中发表的2019年年报显现,陈述期内,苏药厂出产的注射用硫酸阿米卡星销量达907.49万瓶,营收887.14万元。
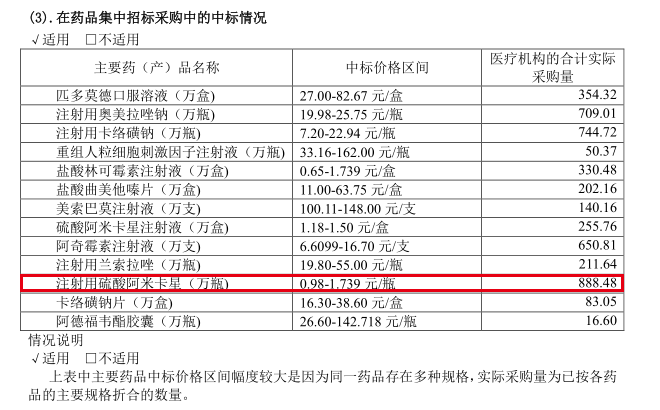
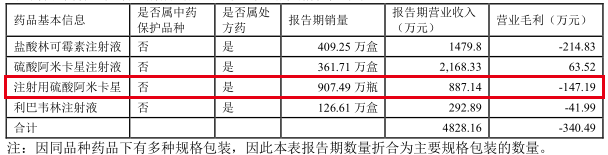
不过,在江苏吴中于7月4日和10日发表的公告中,江苏吴中称,2019年度,苏药厂出产的注射用硫酸阿米卡星(0.2g)出售的收益887.13万元,占公司2019年度经营收入0.42%。问题批次产品所涉种类“注射用硫酸阿米卡星(0.2g)”的出售的收益占公司全体经营收入比重较小,对公司的正常出产经营未形成实质性影响。